- Författare Alex Aldridge aldridge@what-difference.com.
- Public 2023-12-17 13:50.
- Senast ändrad 2025-06-01 07:38.
Den viktigaste skillnaden mellan kvävemonoxid och dikvävepentoxid är att kvävemonoxid är en färglös gas medan dikvävepentoxid är ett vitt fast ämne.
Kvävemonoxid och dikvävepentoxid är kemiska föreningar som innehåller kväve och syre. Dessa är oxider av kväve. De har dock olika kemiska och fysikaliska egenskaper.
Vad är kvävemonoxid?
Kvävemonoxid är en oorganisk förening med den kemiska formeln NO. Vi kallar det kväveoxid eftersom det är en kväveoxid. Det är faktiskt en fri radikal eftersom den har en oparad elektron. Dessutom är det en heteronukleär diatomisk molekyl.
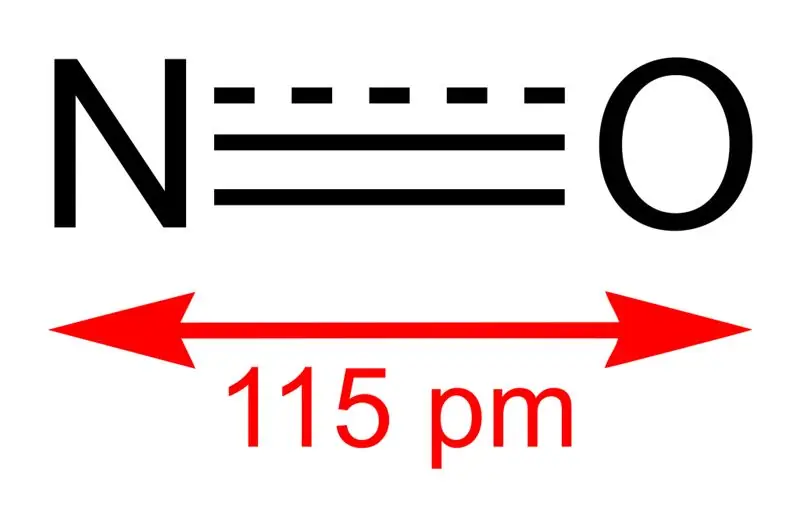
Figur 01: Struktur av kvävemonoxid och bindningslängden mellan N och O
Molmassan för denna förening är 30 g/mol. Det förekommer som en färglös gas. Dessutom är dess smältpunkt -164 °C medan kokpunkten är -152 °C, vilket är mycket små värden jämfört med andra kväveoxider. Vi kan producera denna fria radikal genom oxidation av ammoniak vid 850 °C i närvaro av en platinakatalysator. Men i laboratorieskala kan vi förbereda det genom att reducera utspädd salpetersyra med koppar.
Vad är Dinitrogen Pentoxide?
Dnitrogenpentoxid är en oorganisk förening med den kemiska formeln N2O5 Vi kallar det kvävepentoxid. Det är en binär kväveoxid. Dessutom är det instabilt och kan fungera som ett farligt oxidationsmedel. Den molära massan av föreningen är 108,01 g/mol. Det förekommer en vit fast färg.
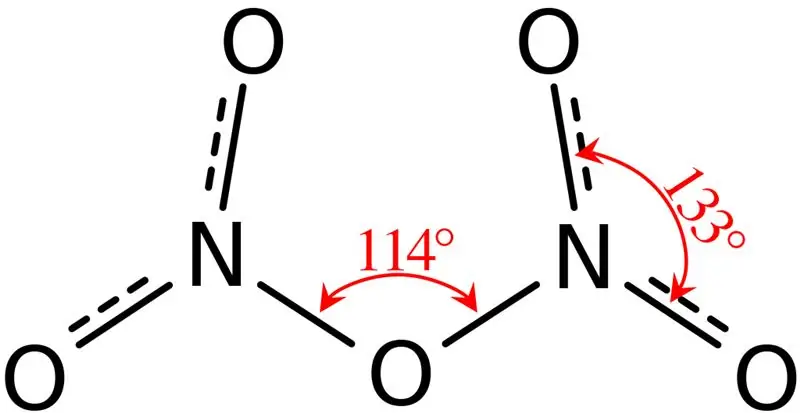
Figur 02: Struktur för dikvävepentoxid
Dessutom är smältpunkten för denna förening 41 °C och vid 47 °C genomgår denna förening sublimering. Denna förening reagerar med vatten och ger salpetersyra. Dessutom är den molekylära formen hos dikvävepentoxidmolekylen plan. Vi kan producera denna förening genom att dehydratisera salpetersyra med fosforpentoxid.
Vad är skillnaden mellan kvävemonoxid och dikvävepentoxid?
Kvävemonoxid är en oorganisk förening med den kemiska formeln NO medan dikvävepentoxid är en oorganisk förening med den kemiska formeln N2O5 Den viktigaste skillnaden mellan kvävemonoxid och dikvävepentoxid är att kvävemonoxid är en färglös gas medan dikvävepentoxid är ett vitt fast ämne. Dessutom kan vi producera kvävemonoxid via oxidation av ammoniak vid 850 °C i närvaro av en platinakatalysator. Produktionen av dikvävepentoxid sker dock via dehydrering av salpetersyra med fosforpentoxid. När man överväger den molekylära formen är kvävemonoxid linjär medan dikvävepentoxid är plan.
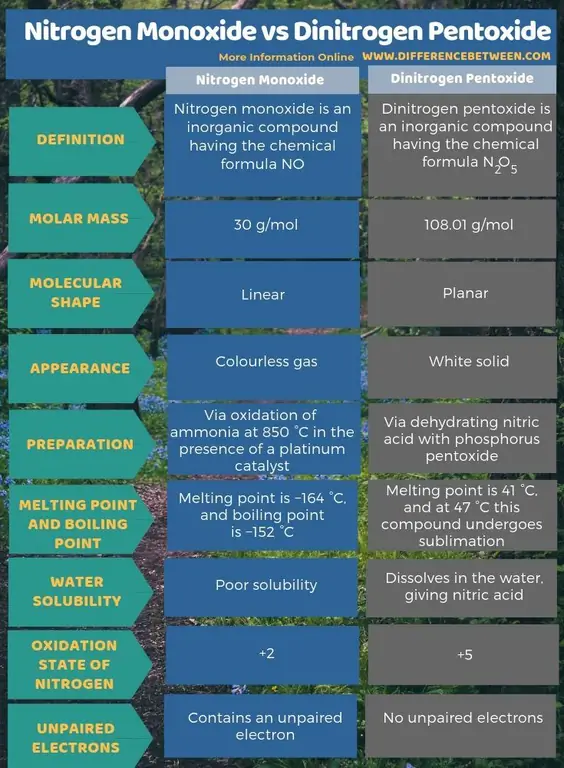
Sammanfattning - Kvävemonoxid vs Dinitrogen Pentoxide
Kvävemonoxid är en oorganisk förening med den kemiska formeln NO medan dikvävepentoxid är en oorganisk förening med den kemiska formeln N2O5 Den viktigaste skillnaden mellan kvävemonoxid och dikvävepentoxid är att kvävemonoxid är en färglös gas medan dikvävepentoxid är ett vitt fast ämne.






